1872年,马克·吐温的《苦行记》出版了。透过这部半自传型游记,我们得以窥见19世纪淘金热时期美国西部万头攒动的繁荣景象。时至今日,黄金储备量已经成为衡量一个国家经济实力的指标之一。十年后,美国阿肯色州政府设立钻石坑公园(Crater of Diamonds State Park),这是世界上唯一一个对公众开放的钻石矿。游客只需支付六美元门票费,就可以自由地寻找钻石并带走任何发现物。据统计,公园开放至今已经发现了25700多颗钻石。
钻石与黄金,堪称大自然赋予我们的宝藏,关于它们还有哪些有趣的知识?我们一起来看看。
一颗纯粹之“心”
钻石,是指具有一定经济价值且经过加工的宝石级金刚石,金刚石主要由碳元素组成;而黄金本质上是一种由化学元素金组成的金属矿物。二者的共同特点显而易见——“自然纯粹”,大部分钻石(部分为人工合成)和几乎全部的黄金均为天然产出,都由某种单一元素组成。人们将这类矿物称为“单质矿物”。
所谓“单质”,在中学化学课上你一定背过它的概念:“单质是由同种元素构成的纯净物”,如铜、铁、氧气等。单质矿物则是指天然形成的、具有一定化学成分与结构的固体单质,它们相对稳定地存在于自然环境中。
单质矿物可分为金属单质矿物和非金属单质矿物。前者包括黄金、白银、铂、铜等大部分金属矿物;后者主要有金刚石、石墨、硫等。单质矿物在地壳中含量极低,但其中的黄金和金刚石等却具有非常重要的经济价值。
钻石真的“恒久远”吗?
或许你早就知道了,我们平时所用的铅笔芯(石墨)和婚戒上的钻石主要成分都是碳元素,可钻石好像占尽了风头:拥有着“一颗永流传”的美称,至今仍是最紧俏、名贵的宝石,常现身于各大拍卖场。为什么成分相同的两种物质会在外观和性质上表现出如此大的差异呢?其中的奥秘就在于碳原子之间的结合方式不同。
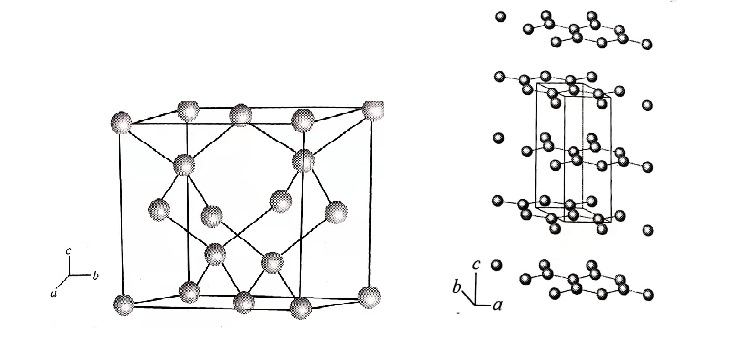
金刚石(左)和石墨(右)的分子结构
上图清晰地显示出了金刚石和石墨内部结构。图中的小球代表碳原子,短棍代表将原子连起来的键。可以看到在金刚石内部,每个碳原子都与其他四个碳原子紧密相连,看起来无懈可击。而石墨中的碳原子成层排列,层与层之间的结合力相对薄弱。我们很容易想象石墨受到外力作用时各层滑动,最后像多米诺骨牌一样断裂的情形。
但,钻石真的“恒久远”吗?
世界上唯一不变的就是改变,即便是在世间已存在33亿年之久的钻石也无法幸免。科学家们的研究结果表明,大部分钻石形成于压力4.5-6.0Gpa(深度约为150-200 km)、温度1100-1500 ℃的环境中。然而,温压条件的变化会改变碳原子之间的结合方式,从而导致钻石与石墨之间相互转化;此外由于碳元素容易被氧化,钻石仅暴露于氧气和800ºC左右的高温就能轻易燃烧生成二氧化碳。
由此可见,结构只决定了矿物一半的性质,另一半则与成分息息相关。这一点在单质矿物的另一位代表“黄金”身上体现得更加淋漓尽致。
“真金不怕火炼”

金的化学符号为Au,源自罗马神话中的黎明女神欧若拉(Aurora),意为闪耀的黎明。从古埃及的金权杖到中国的三星堆金面罩,从首饰到世界性的“硬通货”,自一万两千年前人类发现黄金以来,它便从未走下过“神坛”。黄金之所以拥有如此高的地位,最重要的一点便是其具有良好的稳定性——所谓“真金不怕火炼”。有趣的是,金的熔点并没有我们想象的高,1064ºC。那么所谓的“真金不怕火炼”究竟是否属实?
首先这个说法毋庸置疑。但黄金的稳定性其实是指它不容易与其他物质发生化学反应,即使是在熔融状态下也不会氧化变色、不易挥发,冷却后仍然金光闪闪,甚至不会损失重量。即便是溶于“黄金杀手”王水中,也可以通过置换反应,用比金更活泼的金属元素将其重新提取出来。
钻石似乎总是以棱角分明的面目示人,而黄金可以凹出任何你想要的造型,甚至可以压成万分之一毫米厚的金箔,这得益于它良好的延展性。为什么只有金属单质矿物具有延展性呢?原因还得从它们的基本组成单元“金属原子”入手。金属原子的半径相对较大,也就是说原子核周围的电子离核较远,这样一来就很容易挣脱原子核的束缚重获“自由”,不再只属于某一个原子。所以,当金属受到外力作用时,无论正离子怎么滑动,周围仍然有很多不离不弃的自由电子,这才不会轻易断裂。
无论你是赞叹钻石“宁折不屈”的精神,还是欣赏黄金“随遇而安”的状态,想必看到这里,你已经爱上了拥有纯粹之“心”的单质矿物家族。如果有机会,不妨走进地质博物馆亲自探索体验一番吧,大自然绝不会令你失望。